Giáo án Hóa học Lớp 12 - Bài 1: Este - Phạm Minh Hải
VIII. BÀI TẬP VẬN DỤNG
A- TRẮC NGHIỆM
Câu 1. Chất nào sau đây phản ứng với dung dịch NaOH tạo ra HCOONa và C2H5OH?
A. HCOOCH3. B. CH3COOC2H5.
C. CH3COOCH3. D. HCOOC2H5.
Câu 2. Ester đơn chức tác dụng với NaOH tạo ra 2 muối là
A. Vinyl acetate. B. Methyl benzoate.
C. Phenyl acetate. D. Benzyl acetate.
Câu 3. Một số ester được dùng làm hương liệu, mĩ phẩm, bột giặt là nhờ chúng có tính chất
A. Là chất lỏng dễ bay hơi. B. Có mùi thơm và an toàn với con người.
C. Có thể bay hơi nhanh sau khi sử dụng. D. Đều có nguồn gốc từ thiên nhiên.
Câu 4. Tính chất hóa học quan trọng nhất của ester là
A. Trùng hợp. B. Phản ứng cộng. C. Thủy phân. D. Phản ứng thế.
Câu 5. Phản ứng giữa acid carboxylic với alcohol tạo thành ester gọi là
A. Phản ứng ester hóa. B. Phản ứng cộng.
C. Phản ứng oxi hóa. D. Phản ứng ester hóa
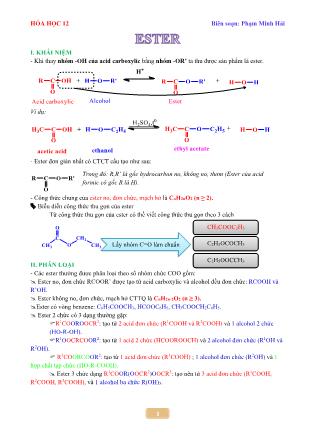
HÓA HỌC 12 Biên soạn: Phạm Minh Hải 1 I. KHÁI NIỆM - Khi thay nhóm -OH của acid carboxylic bằng nhóm -OR’ ta thu được sản phẩm là ester. Ví dụ: - Ester đơn giản nhất có CTCT cấu tạo như sau: - Công thức chung của ester no, đơn chức, mạch hở là CnH2nO2 (n ≥ 2). Biễu diễn công thức thu gọn của ester Từ công thức thu gọn của ester có thể viết công thức thu gọn theo 3 cách II. PHÂN LOẠI - Các ester thường được phân loại theo số nhóm chức COO gồm: Ester no, đơn chức RCOOR’ được tạo từ acid carboxylic và alcohol đều đơn chức: RCOOH và R’OH. Ester không no, đơn chức, mạch hở CTTQ là CnH2n-2O2 (n ≥ 3). Ester có vòng benzene: C6H5COOCH3, HCOOC6H5, CH3COOCH2C6H5. Ester 2 chức có 3 dạng thường gặp: R1COOROOCR2: tạo từ 2 acid đơn chức (R1COOH và R2COOH) và 1 alcohol 2 chức (HO-R-OH). R1OOCRCOOR2: tạo từ 1 acid 2 chức (HCOOROOCH) và 2 alcohol đơn chức (R1OH và R2OH). R1COORCOOR2: tạo từ 1 acid đơn chức (R1COOH) ; 1 alcohol đơn chức (R2OH) và 1 hợp chất tạp chức (HO-R-COOH). Ester 3 chức dạng R1COOR(OOCR2)OOCR3: tạo nên từ 3 acid đơn chức (R1COOH, R2COOH, R3COOH), và 1 alcohol ba chức R(OH)3. Trong đó: R,R’ là gốc hydrocarbon no, không no, thơm (Ester của acid formic có gốc R là H). Lấy nhóm C=O làm chuẩn CH3COOC2H5 C2H5OCOCH3 C2H5OOCCH3 HÓA HỌC 12 Biên soạn: Phạm Minh Hải 2 III. ĐỒNG PHÂN VÀ DANH PHÁP 1. Đồng phân của ester no, đơn chức, mạch hở. Với công thức phân tử là CnH2nO2: - Phân bố số nguyên tử C trên R và R’ của R-COO-R’ (R có thể là H, R’ ≠ H) - Khi số CR/R’ ≥ 3 ≠ → có đồng phân mạch C Lưu ý: CnH2nO2 đơn chức có thể là ester hoặc acid. 2. Danh pháp. Những gốc R’ và RCOO- thường gặp GỐC R’ GỐC RCOO- R’ TÊN GỌI GỐC TÊN GỌI Methyl HCOO- Formate Ethyl CH3COO- Acetate Propyl CH3CH2COO- Propionate Isopropyl CH3CH2CH2COO- Butyrate Vinyl Acrylate Anlyl Methacrylate Phenyl C6H5COO- Benzoate Benzyl Một số ví dụ: HCOOC2H5 ethyl formate CH3COOCH=CH2 vinyl acetate C6H5COOCH3 methyl benzoate CH3COOCH2-C6H5 benzyl acetate CH3COOCH2CH2CH3 propyl acetate CH3COOCH(CH3)2 isopropyl acetate CH3CH2COOC2H5 ethyl propionate CH3CH2CH2COOCH3 methyl butyrate (CH3)2CHCOOCH3 methyl isobutyrate CH2=CHCOOC2H5 Ethyl Acrylate IV. TÍNH CHẤT VẬT LÝ - Trạng thái: lỏng hoặc rắn, rất ít tan (không tan) trong nước. - Nhiệt độ sôi (ts), nhiệt độ nóng chảy (tnc), độ tan: Ester < Alcohol < Acid carboxylic ( có cùng số nguyên tử C, do ester hầu như không tạo ra liên kết Hydro). - Các ester thường có mùi thơm đặc trưng, ví dụ: ✓ Mùi hoa nhài:CH3COOCH2C6H4 ✓ Mùi chuối chín: CH3COOCH2CH2CH(CH3)2 Tên của ester RCOOR’= tên gốc R’ + tên gốc acid RCOO- (nhưng thay đuôi -ic thành -ate) HÓA HỌC 12 Biên soạn: Phạm Minh Hải 3 ✓ Mùi hoa hồng: CH3COOCH2CH=C(CH3)CH2CH2CH=C(CH3)2 ✓ Mùi dứa: ethyl butyrate và ethyl proionate CH3CH2CH2COOCH3 CH3CH2COOC2H5 V. TÍNH CHẤT HÓA HỌC 1. Phản ứng thủy phân. ✓ Ester bị thủy phân trong môi trường acid hoặc base. Thủy phân trong môi trường acid. - Phương trình tổng quát: Ví dụ: Phản ứng ester hóa là phản ứng thuận nghịch. Thủy phân trong môi trường base. Còn gọi là phản ứng xà phòng hóa. Thủy phân ester trong môi trường base là phản ứng không thuận nghịch vì alcohol tạo thành có tính acid yếu hơn tính acid của acid carboxylic. - Phương trình tổng quát: HÓA HỌC 12 Biên soạn: Phạm Minh Hải 4 Ví dụ: 2. Phản ứng của gốc hydrocarbon R, R’. ✓ Phản ứng cộng với dung dịch Br2 (đối với ester không no, mạch hở) → làm mất màu dung dịch Br2. Ví dụ: Hoặc ✓ Phản ứng trùng hợp. ✓ HCOOR có phản ứng tráng gương giống aldehyde Ví dụ: ⎯⎯⎯⎯⎯→3 3 AgNO /NH HCOOR Ag1 mol 2 mol ✓Ester của phenol phản ứng với kiềm dư tạo ra 2 muối và nước. ⎯⎯→ 0t 6 5 6 5 2 HCOOC H + NaOH HCOONa + C H ONa + H O ✓ Phản ứng oxi hóa. Phương trình tổng quát ⎯⎯→ 0t n 2n 2 2 2 2 3n - 2 C H O + O COn + nH O 2 Khi đốt cháy ester no, đơn chức, mạch hở ta luôn có: 2 2 CO H O n = n VI. ĐIỀU CHẾ Phản ứng ester hóa. - Phương trình tổng quát 0 2 4 H SO , t' ' 2 RCOOH + R OH RCOOR + H O Ví dụ: 0 2 4 H SO , t 3 2 5 3 2 5 2 CH COOH + C H OH CH COOC H + H O HÓA HỌC 12 Biên soạn: Phạm Minh Hải 5 Phản ứng riêng điều chế ethyl acetate. 0xt, t 3 3 2 CH COOH + CH CH CH COOCH = CH VII. ỨNG DỤNG VIII. BÀI TẬP VẬN DỤNG A- TRẮC NGHIỆM Câu 1. Chất nào sau đây phản ứng với dung dịch NaOH tạo ra HCOONa và C2H5OH? A. HCOOCH3. B. CH3COOC2H5. C. CH3COOCH3. D. HCOOC2H5. Câu 2. Ester đơn chức tác dụng với NaOH tạo ra 2 muối là A. Vinyl acetate. B. Methyl benzoate. C. Phenyl acetate. D. Benzyl acetate. Câu 3. Một số ester được dùng làm hương liệu, mĩ phẩm, bột giặt là nhờ chúng có tính chất A. Là chất lỏng dễ bay hơi. B. Có mùi thơm và an toàn với con người. C. Có thể bay hơi nhanh sau khi sử dụng. D. Đều có nguồn gốc từ thiên nhiên. Câu 4. Tính chất hóa học quan trọng nhất của ester là A. Trùng hợp. B. Phản ứng cộng. C. Thủy phân. D. Phản ứng thế. Câu 5. Phản ứng giữa acid carboxylic với alcohol tạo thành ester gọi là A. Phản ứng ester hóa. B. Phản ứng cộng. C. Phản ứng oxi hóa. D. Phản ứng ester hóa. Câu 6. Thủy phân ester trong môi trường kiềm còn gọi là A. Xà phòng hóa. B. Hydrate hóa. C. Cracking. D. Lên men. HÓA HỌC 12 Biên soạn: Phạm Minh Hải 6 Câu 7. Ester nào sau đây khi thủy phân cho hai sản phẩm có phản ứng tráng gương: A. HCOOCH2-CH=CH2 B. CH3COOCH=CH2 C. HCOOCH=CH2 D. HCOOC(CH3)=CH2 Câu 8. Thủy phân ester có công thức phân tử C4H8O2 (với xúc tác acid), thu được 2 sản phẩm hữu cơ X và Y. Từ X có thể điều chế trực tiếp ra Y. Vậy chất X là A. rượu methylic B. ethyl acetate C. acid formic D. rượu ethylic Câu 9. Phát biểu đúng là: A. Phản ứng giữa acid và rượu khi có H2SO4 đặc là phản ứng một chiều. B. Tất cả các este phản ứng với dung dịch kiềm luôn thu được sản phẩm cuối cùng là muối và alcohol. C. Khi thủy phân chất béo luôn thu được C2H4(OH)2. D. Phản ứng thủy phân ester trong môi trường acid là phản ứng thuận nghịch Câu 10. Cho các phản ứng (X) + dd NaOH (to ) → (Y) + (Z) (1); (Y) + NaOH (rắn) (to ) → CH4 + (P) (2) CH4 (t o ) → (Q) + H2 (3); (Q) + H2O (xt, to ) → (Z) (4) Các chất (X) và (Z) có thể là những chất được ghi ở dãy nào sau đây. A. CH3COOCH = CH2 và HCHO. B. HCOOCH = CH2 và HCHO. C. CH3COOCH = CH2 và CH3CHO. D. CH3COOC2H5 và CH3CHO. B- TỰ LUẬN Câu 1: Gọi tên các hợp chất có công thức cấu tạo sau: CÔNG THỨC CẤU TẠO TÊN GỌI CH3COOCH3 CH3CH2COOCH3 HCOOC6H5 HCOOCH2CH2CH3 CH2=CHCOOCH3 CH2=CHCOOCH=CH2 CH2=CHCOOCH2C6H5 CH3COOCH(CH3)2 HCOOCH2C6H5 CH3CH2CH2COOC2H5 CH2=C(CH3)COOCH3 C6H5COOCH=CH2 Câu 2: Viết công thức cấu tạo của các hợp chất có tên gọi sau: CÔNG THỨC CẤU TẠO TÊN GỌI Methyl propionate Ethyl acetate Vinyl formate Ethyl acetate Vinyl benzoate Benzyl acetate Methyl acrylate Vinyl methacrylate Anlyl acetate Câu 3: Hoàn thành các phản ứng sau: a. CH3COOCH3 + NaOH → b. HCOOCH2CH2CH3 + NaOH → HÓA HỌC 12 Biên soạn: Phạm Minh Hải 7 c. CH3COOCH=CH2 + NaOH → d. CH3COOCH(CH3)2 + NaOH → e. HCOOCH2C6H5 + NaOH → f. CH3COOC6H5 + NaOH → g. HCOOC6H4CH3 + NaOH → h. (CH3COO)2C2H4 + NaOH → i. (COOCH3)2 + NaOH → k. CH3OOC-COOC6H5 + NaOH → Câu 4: Hoàn thành các phản ứng hóa học sau: a. Ethyl acetate + NaOH → f. Vinyl formate + NaOH→ b. Methyl propionate + NaOH→ g. Ethyl acrylate + NaOH→ c. Isopropyl formate + NaOH→ h. Benzyl acetate + KOH d. Methyl acrylate + KOH→ i. Vinyl benzoate + KOH→ e. Anlyl acetate + KOH→ k. Phenyl acrylate + KOH→ Câu 5: Đốt cháy hoàn toàn 7,4 gam ester X đơn chức thu được 6,72 lít khí CO2 (đktc) và 5,4 gam nước. a. Xác định công thức phân tử của X b. Đun 7,4 gam X trong dung dịch NaOH vừa đủ đến khi phản ứng hoàn toàn thu được 3,2 gam alcohol Y và một lượng muối Z. Viết công thức cấu tạo của X và tính khối lượng của Z. ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................ ........................................................................................................................................................
Tài liệu đính kèm:
 giao_an_hoa_hoc_lop_12_bai_1_este_pham_minh_hai.pdf
giao_an_hoa_hoc_lop_12_bai_1_este_pham_minh_hai.pdf



