Bài giảng Vật lý 12 - Tiết 56, Bài 33: Mẫu nguyên tử Bo
Câu 1. Xét nguyên tử Hidrô đang ở mức năng lượng K. Một phôtôn có năng lượng bằng EM – EK bay đến gặp nguyên tử này. Nguyên tử sẽ hấp thụ phôtôn và chuyển trạng thái như thế nào?
A. Không hấp thụ
B. Hấp thụ nhưng không chuyển trạng thái
C. Hấp thụ rồi chuyển từ K lên L rồi lên M
D. Hấp thụ rồi chuyển thẳng lên M
Bạn đang xem 20 trang mẫu của tài liệu "Bài giảng Vật lý 12 - Tiết 56, Bài 33: Mẫu nguyên tử Bo", để tải tài liệu gốc về máy bạn click vào nút DOWNLOAD ở trên
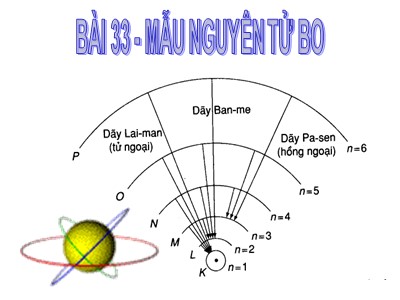
BÀI 33 - MẪU NGUYÊN TỬ BO Câu 1 : Hiện tượng quang-phát quang là gì ? Chất phát quang là gì ? KIỂM TRA BÀI CŨ Câu 2 : Phân biệt hiện tượng huỳnh quang và hiện tượng lân quang Trả lời Câu 1 : Hiện tượng quang-phát quang là gì ? Chất phát quang là gì ? Trả lời: Hiện tượng quang - phát quang là hiện tượng một số chất có khả năng hấp thụ ánh sáng có bước sóng này để phát ra ánh sáng có bước sóng khác. Chất có khả năng phát sáng là chất phát quang Trả lời Câu 2 : Phân biệt hiện tượng huỳnh quang và hiện tượng lân quang ? Trả lời: + Huỳnh quang là sự phát quang của các chất lỏng và khí có đặc điểm là ánh sáng phát quang thời gian tắt rất nhanh sau khi tắt ánh sáng kích thích. + Lân quang là sự phát quang của các chất rắn có đặc điểm là ánh sáng phát quang có thể kéo dài một khoảng thời gian nào đó sau khi tắt ánh sáng kích thích. Quang phổ vạch phát xạ của Hyđrô trong vùng ánh sáng nhìn thấy gồm các vạch màu: Đỏ , Lam , Chàm , Tím Trả lời: Quang phổ của Hyđrô là loại quang phổ vạch. ------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------ Câu 3. Quang phổ của hyđrô là loại quang phổ gì? NỘI DUNG BÀI MỚI I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ 1. Tiên đề về các trạng thái dừng: 2. Tiên đề về sự bức xạ và hấp thụ năng lượng của nguyên tử: III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ BÀI 33 - MẪU NGUYÊN TỬ BO MẪU NGUYÊN TỬ BO Tiết: 56 I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ Thomson - Mô Hình Nguyên tử của Thomson là quả cầu đặc mang điện tích dương,các electron chuyển động trong quả cầu đó. MẪU NGUYÊN TỬ BO Tiết: 56 I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ - Năm 1911 Rutherford đã đề xướng mẫu hành tinh nguyên tử. - Nội dung Nguyên tử gồm các electron mang điện tích âm chuyển động xung quanh hạt nhân mang điện tích dương với những quỹ đạo khác nhau theo từng lớp. RUTHERFORD - Mô hình mẫu nguyên tử hành tinh của Rodonfor: bao gồm các electron mang điện tích âm chuyển động xung quanh hạt nhân mang điện tích dương với những quỹ đạo khác nhau, theo từng lớp. MẪU NGUYÊN TỬ RODONFOR Mẫu nguyên tử Hành tinh rodonfor Mẫu nguyên tử của Thomas và Rodonfor trên đều gặp khó khăn trong việc giải thích tính bền vững của nguyên tử và sự tạo thành quang phổ vạch của nguyên tử Hyđrô. Nên Bo đã vận dụng thuyết lượng tử và Mẫu nguyên tử hành tinh để đưa ra mẫu Nguyên tử Bor Tiết: 56 I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ - Năm 1913 khi dùng thuyết lượng tử để giải thích sự tạo thành quang phổ của hiđrô, Bo đã giữ mô hình hành tinh nguyên tử Rơ-dơ-pho và đề ra hai giả thuyết gọi là hai tiên đề Bo về cấu tạo nguyên tử. Niels Bohr Như vây: Mẫu nguyên tử Bo bao gồm mô hình hành tinh nguyên tử và hai tiên đề của Bo. Bài 33 - MẪU NGUYÊN TỬ BO Niels Bohr (1885 – 1962) nhà vật lý học Đan Mạch. Năm 1913 Bor đã giữ mô hình hành tinh nguyên tử Rơ-dơ-pho và đề ra hai giả thuyết gọi là hai tiên đề Bo về cấu tạo nguyên tử. Tiết: 56 I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ Bài 33 - MẪU NGUYÊN TỬ BO I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ - Mẫu nguyên tử Bo bao gồm mô hình hành tinh nguyên tử và hai tiên đề của Bo. II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ Tiết: 56 1. Tiên đề 1( về trạng thái dừng) Bài 33 - MẪU NGUYÊN TỬ BO 1. Tiên đề về 1(trạng thái dừng) - Nguyên tử chỉ tồn tại trong một số trạng thái có năng lượng xác định gọi là các trạng thái dừng. Khi ở trạng thái dừng thì nguyên tử không bức xạ. - Trong các trạng thái dừng của nguyên tử, electron chỉ chuyển động quanh hạt nhân trên những quỹ đạo có bán kính xác định gọi là các quỹ đạo dừng Trong các trạng thái dừng của nguyên tử electron chuyển động như thế nào ? I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ Tiết: 56 Bài 33 - MẪU NGUYÊN TỬ BO HẠT NHÂN 4r 0 9r 0 Quỹ đạo L Quỹ đạo K Quỹ đạo M Trang thái cơ bản Trang thái kích thích Bán kính thứ nhất Bán kính thứ hai Bán kính thứ ba Bài 33 - MẪU NGUYÊN TỬ BO r 0 Trang thái kích thích Mô hình Mẫu nguyên tử Hidro của Bor Với nguyên tử Hidro Lượng tử số 1 2 3 4 5 6 Tên quỹ đạo K L M N O P Bán kính quỹ đạo r 0 4r 0 9r 0 16r 0 25r 0 36r 0 Nguyên tử Hidro có một nhân(+) và một e(-) chuyển động xung quanh nhân với những quỹ đạo dừng có năng lượng xác định và khác nhau, kí hiệu K,L,M,N,O,P, Tương úng từ 1,2,3,4,5,6, ; với quỹ đạo trong cùng ở mức có năng lượng thấp nhất (K) có bán kính r 0 (quỹ đạo cơ bản, mà e bền nhất). r 0 = 5,3.10 -11 m; r n = n 2 r 0 I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ Tiết: 56 1. Tiên đề về trạng thái dừng Bài 33 - MẪU NGUYÊN TỬ BO Khi nào thì nguyên tử bức xạ năng lượng ? = E n - E m E n E m I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ MẪU NGUYÊN TỬ BO Tiết: 56 Mức ngăng lượng cao Mức ngăng lượng thấp 2. Tiên đề 2(về sự bức xạ , hấp thụ năng lượng của nguyên) tử. - Khi nguyên tử chuyển từ trạng thái dừng có năng lượng E n sang trạng thái dừng có năng lượng thấp hơn E m thì nó phát ra phô tôn có năng lượng đúng bằng hiệu E n - E m = hf nm = E n - E m I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ MẪU NGUYÊN TỬ BO Tiết: 56 = E n - E m E m E n Ti ế t 57 MẪU NGUYÊN TỬ BO = E n - E m Mức ngăng lượng cao Mức ngăng lượng thấp Ngược lại, nếu nguyên tử đang ở trạng thái dừng có năng lượng E m thấp mà hấp thụ được một phô tôn có năng lượng đúng bằng hiệu E n - E m thì nó chuyển lên trạng thái dừng có năng lượng cao hơn E n : = hf nm = E n - E m 2. Tiên đề về sự bức xạ và hấp thụ năng lượng của nguyên tử. I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ MẪU NGUYÊN TỬ BO Tiết: 56 Ti ế t 57 MẪU NGUYÊN TỬ BO 2. Tiên đề về sự bức xạ và hấp thụ năng lượng của nguyên tử. I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ =hf nm E n E m =hf nm Mức ngăng lượng cao Mức ngăng lượng thấp Ti ế t 56 MẪU NGUYÊN TỬ BO 2. Tiên đề về sự bức xạ và hấp thụ năng lượng của nguyên tử. I. MÔ HÌNH HÀNH TINH NGUYÊN TỬ II. CÁC TIÊN ĐỀ CỦA BO VỀ CẤU TẠO NGUYÊN TỬ Câu C2 C2. Nếu phô tôn có năng lượng lớn hơn hiệu E n – E m thì nguyên tử cũng không hấp thụ được. - Năm 1885, khi nhìn bằng lăng kính, Balmer đã nhìn thấy ánh sáng từ bốn bước sóng tương ứng với 4 vạch sáng: đỏ (656.3 nm), lam (486.1 nm), chàm (434.0 nm ), tím(412.0 nm) của nguyên tử Hidro. Ông gọi 4 vạch đó lần lượt là H α , H β , H γ , H δ H δ H γ H β H α III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 1. Đặc điểm quang phổ của Hyđrô - 21 năm sau, 1906 - 1914 Theodore Lyman đã phát hiện ra rằng quang phổ vạch hidro không phải chỉ có 4 vạch mà còn có một số vạch thuộc phần tử ngoại H δ H γ H β H α III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 1. Đặc điểm quang phổ của Hyđrô - Năm 1908, nhà vật lý người Áo-Đức, Paschen đã quan sát thấy trong quang phổ vạch của nguyên tử hidro còn có một số vạch thuộc vùng hồng ngoại. Louis Karl Heinrich Friedrich Paschen (January 22, 1865 - February 25, 1947) III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 1. Đặc điểm quang phổ của Hyđrô K L M N O P Giải thích Đặc điểm quang phổ của Hyđrô Mức ngăng lượng cao Mức ngăng lượng thấp L M N O P H H H H Lyman Balmer Pasen K vùng hồng ngoại vùng tử ngoại vùng Á S nhìn thấy Giải thích Đặc điểm quang phổ của Hyđrô Mức ngăng lượng cao Mức ngăng lượng thấp L M O P N = E n - E m -E0/1 2. Giải thích quang phổ của Hyđrô phát xạ Giải thích Đặc điểm quang phổ của Hyđrô L M O P N = E n - E m 2. Giải thích quang phổ của Hyđrô phát xạ Giải thích Đặc điểm quang phổ của Hyđrô L M O P N = E n - E m 2. Giải thích quang phổ của Hyđrô phát xạ Giải thích Đặc điểm quang phổ của Hyđrô L M O P N = E n - E m ------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------------ 2. Giải thích quang phổ của Hyđrô phát xạ Giải thích Đặc điểm quang phổ của Hyđrô III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 1. Giải thích quang phổ của Hyđrô - Khi electron chuyển từ mức năng lượng cao về mức năng lượng thấp thì nó phát ra một phô tôn có năng lượng hoàn toàn xác định: = hf nm = E n - E m III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 2. Đặc điểm quang phổ của Hyđrô L M O P N = E n - E m 3. Giải thích quang phổ của Hyđrô hấp thụ L M O P N = E n - E m 3. Giải thích quang phổ của Hyđrô hấp thụ L M O P N = E n - E m 3. Giải thích quang phổ của Hyđrô hấp thụ L M O P N = E n - E m 3. Giải thích quang phổ của Hyđrô hấp thụ III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 3. Giải thích quang phổ hấp thụ của Hyđrô Khi nguyên tử Hidro đang ở một mức năng lượng thấp nào đó mà nó nằm trong một chùm sáng trắng, trong đó các phô tôn . Do đó quang phổ liên tục xuất hiện một vạch tối. III. QUANG PHỔ PHÁT XẠ VÀ HẤP THỤ CỦA NGUYÊN TỬ HIĐRÔ MẪU NGUYÊN TỬ BO Tiết: 56 4. Ưu và nhược điểm của mẫu nguyên tử Bo *Ưu điểm: - Tìm ra được cấu trúc nguyên tử Hiđrô và các iôn tương tự (He + ; Li 2+ ). Giải thích được sự tạo thành quang phổ vạch của Hiđrô, tính chính xác bước sóng của các vạch quang phổ của Hiđrô. *Nhược điểm: - Chưa đi vào các quy tắc đặc thù của thế giới vi mô (quy tắc lượng tử, quy tắc lựa chọn, hệ thức bất định, ) - Chưa đề cập đến những đặc điểm riêng của thế giới vi mô (lưỡng tính sóng hạt, các số lượng tử, spin, .) Câu 1 . Xét nguyên tử Hidrô đang ở mức năng lượng K . Một phôtôn có năng lượng bằng E M – E K bay đến gặp nguyên tử này. Nguyên tử sẽ hấp thụ phôtôn và chuyển trạng thái như thế nào? A. Không hấp thụ B . Hấp thụ nhưng không chuyển trạng thái C. Hấp thụ rồi chuyển từ K lên L rồi lên M D . Hấp thụ rồi chuyển thẳng lên M E K E L E M = E M - E K CỦNG CỐ A. Hình dạng quỹ đạo của các electron B. Lực tương tác giữa electron và hạt nhân nguyên tử C. Trạng thái có năng lượng ổn định D. Mô hình nguyên tử có hạt nhân CỦNG CỐ Câu 2: Mẫu nguyên tử Bo khác mẫu nguyên tử Rơ-dơ-pho ở điểm nào dưới đây ? BÀI TẬP VỀ NHÀ . BT 6, 7/trang 169 SGK Tr¶ lêi: Nguyªn tö kh«ng ph¶i lóc nµo còng bøc x¹. VËy nguyªn tö bøc x¹ khi nµo? Gi¶ thuyÕt nµy hoµn toµn tr¸i ngîc víi thuyÕt cæ đ iÓn h·y chØ ra ®iÒu ®ã ? n = 1 2 3 4 K L M N 2 3 4 K L M N n = 1 2 3 4 K L M N n = 1
Tài liệu đính kèm:
 bai_giang_vat_ly_12_tiet_56_bai_33_mau_nguyen_tu_bo.ppt
bai_giang_vat_ly_12_tiet_56_bai_33_mau_nguyen_tu_bo.ppt



